卫康生物:李兰娟院士揭示肠道菌群与健康奥秘
发布: 2026-04-17 09:58:12 作者: 佚名 来源: 卫康生物
你或许好奇:肠道里百万亿级的微生物,为何能影响全身健康?
2014年,中国工程院李兰娟院士团队在《Nature》发表重磅研究,首次揭示肝硬化患者肠道菌群的基因秘密,创建了世界首个肝硬化肠道菌群基因集。这一成果不仅入选中国高等学校十大科技进展,更印证了她首创的“感染微生态理论”——肠道微生态失衡,正是许多慢性病的隐形推手。
肠道微生态:
人体健康的“全身指挥中心”

肠道菌群就像一个复杂的“生态社区”,住着百万亿级微生物,比人体细胞总数还多10倍。李兰娟院士曾形象比喻:“人类肠道菌群就好比一个热带雨林生态系统,需要尽可能多的多样性。”肠道菌群组成越丰富多样的人,其健康状况也越好。
李兰娟院士带领的传染病重症诊治全国重点实验室发现,这个社区并非简单的“居民集合”,而是参与“代谢—免疫—神经—器官互作”的调控网络。中华医学会老年医学分会制定的《肠道微生态制剂老年人临床应用中国专家共识》明确指出,李兰娟院士强调:肠道菌群不仅影响消化吸收,更会牵动免疫、代谢和神经系统,是“衰老链条”的关键环节。
在这个生态系统中,有益菌如双歧杆菌、乳杆菌,是社区里的“建设者”,它们分泌的短链脂肪酸能修复肠黏膜屏障,就像给肠道筑起坚固的“城墙”;而条件致病菌则是“破坏者”,一旦过度增殖,就会打破平衡。健康状态下,两者和平共处,但当这个社区秩序混乱,肠道屏障就会出现“漏洞”,未被完全消化的食物大分子或毒素便会进入血液,引发全身慢性炎症——这正是慢病的“导火索”。
菌群失衡:慢病滋生的“隐形温床”

权威期刊《Gut》的数据令人警醒:超过90%的慢性病,从肥胖、糖尿病到自身免疫病,都与肠道菌群失衡相关。李兰娟院士团队的研究进一步证实,菌群失衡引发的慢性低度炎症,是多种慢病共同的病理基础。正如专家共识所指出的,这种“菌群老化”会引发慢性低度炎症、肠屏障受损与免疫功能紊乱,它往往是糖尿病、动脉硬化、骨质疏松、认知障碍等疾病的隐性起点。
近年来一系列权威研究提供了确凿证据:
01 心血管疾病:
《Nature》最新研究发现,一种由肠道微生物产生的代谢物“咪唑丙酸”,不仅仅是疾病的“旁观者”,更是直接驱动动脉粥样硬化的“肇事者”。
02 神经退行性疾病:
帕金森病、阿尔茨海默病患者,往往在神经症状出现前数年便已发生肠道菌群变化。老年高血压患者肠道菌群研究也证实,菌群失调与系统性炎症水平密切相关。
03 代谢性疾病:
中国疾控中心对15省3224人的调查发现,肠道菌群与血压、血糖等慢病指标直接相关;一项系统综述明确指出,肠道菌群已成为代谢综合征(包括胰岛素抵抗、脂质失衡、中心性肥胖和高血压)病理生理学的核心贡献因素。
这些研究共同证明:肠道菌群不是慢病的“旁观者”,而是“参与者”甚至“始作俑者”。
临床实证:微生态干预改写慢病结局
近年来的临床研究进一步证实,靶向肠道菌群的干预正在改写慢病治疗格局。
2025年,新西兰奥克兰大学团队发表了一项长达4年的随访研究,结果显示:代谢综合征患者接受一次粪菌移植治疗后,代谢健康改善持续至少4年,糖尿病和心脏病风险显著降低。
李兰娟院士团队在2025年发表于《Engineering》期刊的研究中,从中国大样本人群中筛选出10种能够表征整个肠道菌群的优势菌,构建了简便高效的微生态平衡评估方法。研究发现,肝硬化患者与健康人群的菌群构成存在显著差异,且肠道菌群与肝硬化严重程度相关。
同年,李兰娟院士团队还在《Microbiome》期刊发表了FMT“双重优化”策略,提出从“寻找好供体”向“制造好供体”的范式转变,推动FMT向精准化、可控化方向发展。
科学守护:给肠道菌群的“健康处方”
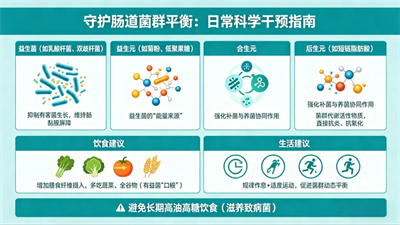
守护肠道菌群平衡,无需复杂技术,日常行为即可见效。专家共识提出了四类科学干预手段:
益生菌(如乳酸杆菌、双歧杆菌):
有助于抑制有害菌生长,维持肠黏膜屏障
益生元(如菊粉、低聚果糖):
是益生菌的“能量来源”
合生元:
将两者结合,强化补菌与养菌的协同作用
后生元:
菌群代谢产生的活性物质(如短链脂肪酸),可直接发挥抗炎、抗氧化功效
饮食上,增加膳食纤维摄入,多吃蔬菜、全谷物,它们是有益菌的“口粮”;同时避免长期高油高糖饮食,这类食物会滋养致病菌。规律作息与适度运动,能促进菌群动态平衡。
李兰娟院士的研究揭示了一个深刻的真理:肠道微生态是健康的底层逻辑。正如李兰娟院士所说:“肠道微生态一旦被破坏,就会牵动免疫、代谢和神经系统。”当我们呵护好肠道里的“隐形军团”,它们就会成为慢病防控的“天然盟友”,这正是现代健康管理的核心密码。
上一篇:下一篇: 卫康生物2026一季度总结暨二季度启动会...
今日新闻头条
我也说两句
已有评论 0 条 查看全部回复











